El método que aquí se describe es el llamado método de Kjeldhal.
Entendemos per proteína bruta el nitrógeno total de la muestra expresado como proteína. El método no es apto para aquellas substáncias que presentan enlaces N-N, NO y NO2.
Se somete la muestra a un ataque con ácido sulfúrico concentrado, durante el cual el nitrógeno pasa a forma amoniacal (como sulfato amónico); el amonio del sulfato amónico pasa a amoníaco libre por tratamiento con hidróxido de sodio:
(NH4)2SO4 + 2NaOH --> Na2SO4 + 2NH3 + 2H2O
y el amoníaco así formado se separa mediante destilación y se recoge sobre una cantidad exactamente conocida de disolución ácida titulada. El amoníaco formado se determina mediante valoración del exceso de ácido titulado.
MATERIAL
Aparato semimicro Kjeldhal según esquema adjunto.
Balanza analítica.
Batería digestora de mantas eléctricas.
Bureta de 25 ml.
Campana-vitrina extractora.
Frasco lavador.
Matraz erlenmeyer de 100 ml ó de 250 ml.
Matraz Kjeldhal, forma pera de cuello largo de 100 ml.
Pipetas de 25 ml y de 5 ml.
Probeta de 25 ml.
REACTIVOS
ácido clorhídrico 0'1 N, titulado.
ácido sulfúrico concentrado.
Agua destilada.
Disolución de hidróxido de sodio 50% p/v.
Indicador mixto Shiro-Thasiro.
Mezcla catalítica.
Papel de fumar.
Preparación de reactivos:(pa es pureza analítica)
INDICADOR MIXTO.- Mezclar dos partes de solución de rojo de metilo al 0'2 % con una parte de azul de metilo al 0'2 %, y dos de alcohol etílico del 96. Guardar en frasco topacio. Viraje: rojo violáceo a verde-gris.
SOLUCIÓN DE SOSA AL 50 % P/V.- Disolver 500 gramos de NaOH y 50 gramos de tiosulfato de sodio en agua hasta 1 litro, agitando continuamente y enfriando simultáneamente el recipiente en baño de agua fría, con cuidado de no salpicar.
MEZCLA CATALÍTICA.- Mezclar y homogeneizar 150 gramos de sulfato de potasio pa, 4 gramos de óxido cúprico pa y 12 gramos de sulfato cúprico cristalizado pa. Molturar hasta reducir a polvo fino y homogeneizar de nuevo.
METODOLOGíA
1.- Pesar, en papel de fumar, al cual se le habrá eliminado la parte engomada, una cantidad de muestra molturada y homogeneizada que contenga entre 100 y 120 miligramos de proteína bruta.
2.- Pasar la muestra, envuelta en el papel de fumar, al interior del matraz Kjeldhal.
3.- Añadir alrededor de 2'5 gramos de mezcla catalítica y 6 ml de ácido sulfúrico concentrado. Tapar el matraz con un embudo pequeño.
4.- Calentar la muestra con la batería calefactora en vitrina-campana y poner en marcha el extractor; el calentamiento será suave durante los 5 primeros minutos y fuerte a continuación. Continuar el calentamiento hasta que el líquido sea de color verde-azul claro y totalmente transparente. El tiempo de digestión varia según el tipo de muestra (alrededor de ¾ de hora).
5.- Enfriar, y cuando el líquido esté frío, añadir entre 5 y 10 ml de agua destilada, lavando el cuello del matraz.
6.- Pasar el líquido al destilador, lavando el matraz tres o cuatro veces con pequeñas cantidades de agua destilada.
7.- Con todas las llaves del aparato cerradas, añadir de 20 a 25 ml de disolución de sosa; pasar al cuerpo del destilador dejando una pequeña cantidad en el embudo que actuará como cierre hidráulico.
8.- Lavar el embudo con agua destilada, dejando pasar todo el líquido de lavado, excepto una pequeña porción que actuará de cierre hidráulico.
9.- Destilar y recoger el amoníaco en un erlenmeyer de 100 ml, sobre 25 ml de HCl 0'1 N titulado, con unas gotas del indicador mixto.
10.- Después de recoger unos 40-50 ml de destilado, comprobar que ya no destila amoníaco, mediante una tira de papel indicador.
11.- Valorar el exceso de ácido titulado con disolución titulada de NaOH 0'1 N.
12.- Periódicamente, efectuar un blanco con papel de fumar del tipo empleado en las determinaciones. El volumen correspondiente de ácido titulado empleado se considera consumido como blanco. Es preciso que el papel de fumar sea siempre de la misma marca y tipo; en caso contrario, deberá efectuarse una comprobación en blanco.
13.- Una vez finalizado el proceso, deberá procederse a la limpieza del aparato, procediendo al efecto de la siguiente forma: continuando el paso de vapor y con las llaves cerradas, llenar con agua destilada el embudo; el extremo del refrigerante se sumerge en unos 100 ml de agua destilada. Se interrumpe la producción de vapor
y se abre ligeramente la llave del embudo, cerrándola antes que toda el agua pase al interior del aparato. La reducción de presión succiona el agua del vaso al interior del aparato, lavándolo. La llave del tubo de purga se abre a continuación a fin de vaciar el líquido recogido en la camisa exterior. Se repite el proceso volviendo a permitir la producción de vapor.
CÁLCULOS
Para expresar el resultado como contenido en nitrógeno:
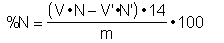
en donde:
% N = Contenido de nitrógeno de la muestra, expresado en %
V = Volúmen, en ml del ácido titulado
N = Normalidad del ácido titulado.
V'= Volúmen de base titulada empleado en la valoración.
N'= Normalidad de la base empleada en la valoración.
m = Masa pesada de muestra, en miligramos.
si la normalidad de la base = normalidad del ácido = 0'1000 N y el volúmen del ácido es de 25 ml, la expresión anterior quedará de la forma:
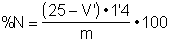
para expresar el resultado en contenido de proteína bruta, debe multiplicarse el contenido de nitrógeno por un factor que depende del tipo de muestra y que, en general, tiene un valor que oscila alrededor de 6'25.
OBSERVACIONES
Hay otros tipos de mezclas catalíticas (las más empleadas, además de la mencionada en esta Práctica, son a base de selenio o de mercurio). El objetivo de las mezclas catalíticas es el de reducir el tiempo de digestión, que de no usarse mezcla catalítica, se prolongaría durante varias horas. Debe tenerse en consideración que la mayoría de las mezclas catalíticas son tóxicas y hay que tomar las precauciones de no respirar sus vapores y evitar el contacto con la piel.
Para la dosificación de la mezcla catalítica, podemos hacer una estimación experimental del volúmen aproximado del peso indicado (2'5 gramos en este caso) y así evitarnos el pesarla cada vez que procedamos a un análisis.
Aparato Kjeldhal semimicro para determinación de nitrógeno:
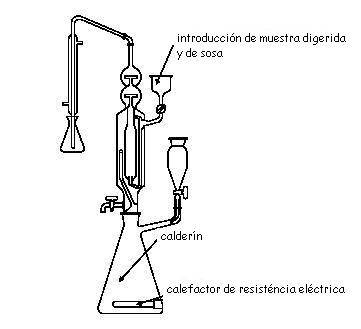
Cuestionario 5.1.- Determinación de la proteína bruta
1.- Escribir las reacciones que tienen lugar a lo largo de la Práctica.
2.- Hacer el esquema gráfico del procedimiento analítico.
3.- Deducir razonadamente la fórmula utilizada en los cálculos.
4.- Calcular el factor de conversión de nitrógeno a proteína para una muestra de un pequeño péptido formado por la siguiente secuencia de aminoácidos:
glicina-alanina-glicina-glicina
5.- Confeccionar el correspondiente "boletín de análisis".
Extraído de http://www.xtec.es/~ffernan5/castellano/05001.htm




 bobquim.
bobquim.